
La maladie de Charcot est une pathologie neurodégénérative grave et rare. Progressive, elle entraîne la paralysie des patients ainsi qu’un pronostic sombre. Comment expliquer et reconnaître la maladie de Charcot ? Quelle prise en charge et quels espoirs concernant la recherche médicale ? Focus.
Comprendre la maladie de Charcot
Également appelée la sclérose latérale amyotrophique (SLA), la maladie de Charcot est une pathologie neurodégénérative grave et progressivement handicapante, puisque les muscles impliqués dans la motricité volontaire se paralysent peu à peu. La production de sons et la déglutition finissent également par être affectées. L’issue de cette maladie est fatale après 3 à 5 ans d’évolution en moyenne, en raison de l’atteinte des muscles respiratoires. Près de 7000 cas sont recensés en France, dont 1000 nouveaux cas par an, selon l’Institut du cerveau.
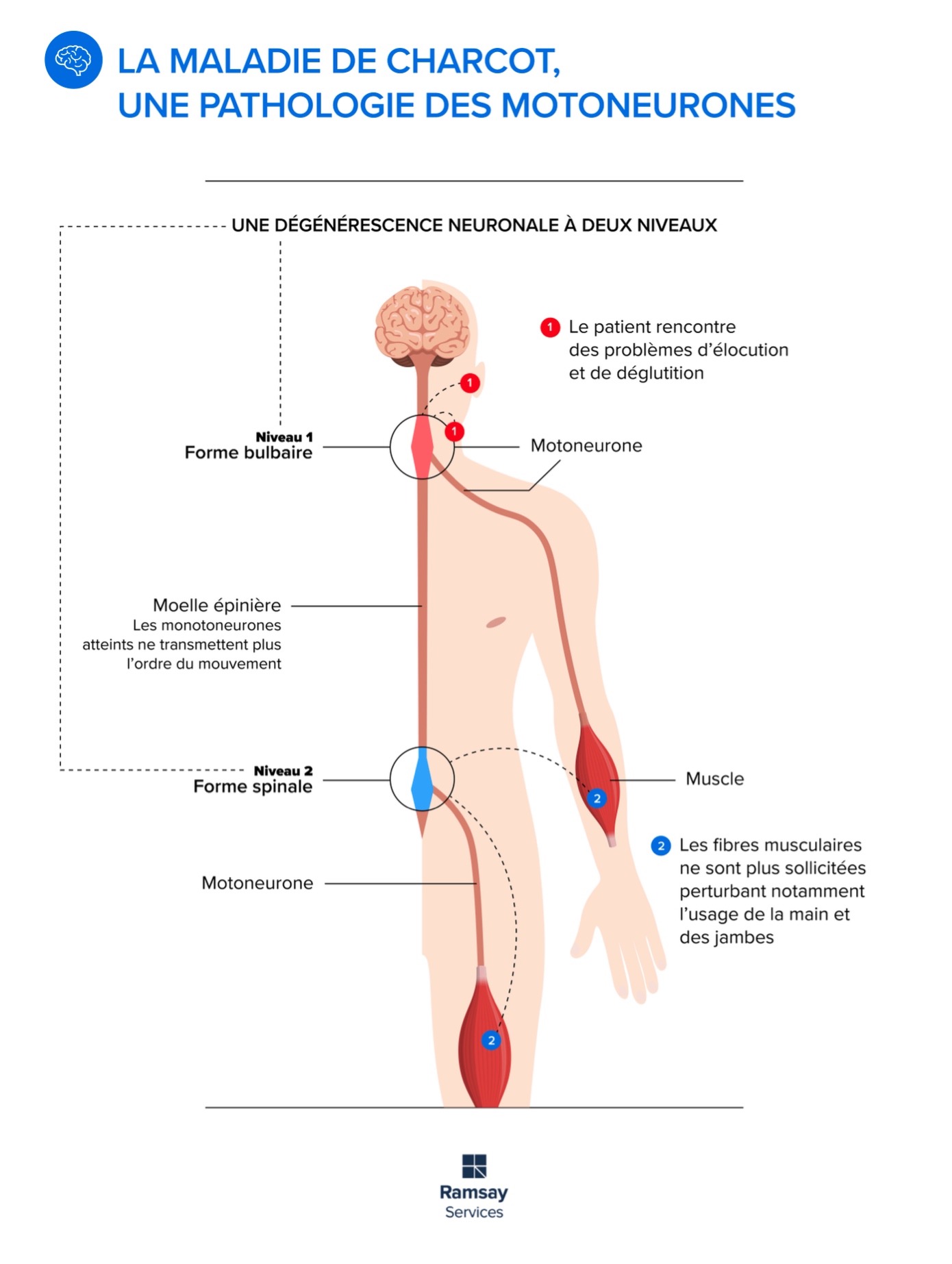
La maladie de Charcot est également surnommée « maladie du motoneurone », en raison de son fonctionnement. En effet, les motoneurones, ces cellules nerveuses qui dirigent et contrôlent les muscles volontaires, meurent progressivement. Il s’agit autant des motoneurones « centraux », dans le cerveau, que des motoneurones périphériques, situés dans le tronc cérébral et la moelle épinière.
Maladie de Charcot : une origine génétique avant tout
Bien qu’elle soit multifactorielle, l’origine de la maladie de Charcot est avant tout génétique : 10% des SLA sont dites « familiales », d’après l’Inserm. Pendant un certain temps, un seul gène (le SOD1) était considéré comme responsable de l’apparition de la maladie, lorsqu’il mutait. Mais une trentaine d’autres gènes ont été identifiés comme jouant un rôle dans la survenue de la SLA, dont un (le C9ORF72) dont la mutation est observée dans 40% des cas de formes familiales.
Quand la génétique familiale n’est pas impliquée (dans la majorité des cas), la maladie de Charcot est dite « sporadique », sans doute liée à la mutation aléatoire d’un gène.
Des causes environnementales sont suspectées mais leur implication reste à confirmer :
- Le tabagisme ;
- Le sport de haut niveau ;
-
L’exposition prolongée à certains pesticides, métaux lourds et à une toxine présente dans certaines algues.
Maladie de Charcot : comment la reconnaître ?
Cette pathologie apparaît généralement entre 50 et 70 ans et parfois plus tôt quand elle est d’origine familiale. Lorsque les motoneurones centraux sont d’abord touchés (dans 30% des cas environ), la maladie débute au niveau du tronc cérébral et se manifeste par des difficultés à déglutir ou à articuler : il s’agit de forme à début bulbaire.
Autre possibilité, si les motoneurones périphériques sont atteints en premier, la maladie apparaît sous forme de faiblesse ou de gêne ressentie au niveau d’un bras, d’une main ou d’une jambe : c’est une forme à début spinal.
Comment évolue la maladie de Charcot ?
La maladie évolue ensuite progressivement, mais en s’intensifiant : des contractures et des raideurs des muscles et des articulations apparaissent. D’autres muscles sont ensuite atteints. Puis, ces derniers finissent par fondre et la marche, la préhension des objets, la déglutition et l’articulation sont gênées par divers troubles de la coordination. A un stade avancé de la maladie, les muscles respiratoires finissent par être atteints à leur tour, ce qui précipite l’aggravation de la SLA et son issue fatale.
Le diagnostic de la maladie de Charcot
Dans le parcours diagnostique, le neurologue commence par éliminer toute suspicion de maladie neurodégénérative et touchant les motoneurones. Pour cela, il prescrit divers examens neurologiques et cliniques :
- Un électromyogramme qui consiste à enregistrer les signaux électriques qui circulent entre les neurones et les muscles. Cet examen confirme donc la dénervation motrice des muscles.
- Une IRM cérébrale.
- Un test génétique, réalisé par une simple prise de sang en cas d’antécédents familiaux.
D’autres examens plus spécifiques peuvent également être prescrits. Leur objectif ? Détecter des signes de neurodégénérescence musculaire, d’atteinte bulbaire, mais aussi des pathologies ou symptômes associés.
Maladie de Charcot : quels traitements ?
A ce jour, il n’existe pas de traitement permettant de soigner la maladie de Charcot. Seuls les symptômes sont ciblés et leur progression peut être ralentie à l’aide de divers traitements, le tout faisant l’objet d’une prise en charge pluridisciplinaire :
- Des séances de kinésithérapie ;
- Des médicaments antispastiques peuvent être prescrits pour lutter contre les troubles moteurs ;
- Des antalgiques contre les douleurs ;
- Un suivi assuré par un médecin nutritionniste pour lutter contre la dénutrition ;
- Un suivi assuré par un orthophoniste concernant les troubles de la parole ;
- Un accompagnement psychologique pour le patient et ses proches ;
- Un médicament efficace pour ralentir la progression des symptômes : le riluzole ;
-
Enfin, un système de ventilation non invasive (VNI) permet de suppléer la fonction respiratoire lorsqu’elle commence à décliner.
Maladie de Charcot : où en est la Recherche ?
La maladie de Charcot est de plus en plus considérée comme un syndrome, en raison des multiples caractéristiques qui peuvent lui être associées. Autrement dit, plusieurs pathologies du motoneurone pourraient être regroupées sous l’appellation de SLA. Une perspective qui pourrait expliquer l’échec de nombreux essais cliniques pour trouver un traitement contre la maladie de Charcot. C’est un objectif de la recherche à part entière : répartir les patients en différents groupes, en fonction de caractéristiques de la maladie communes.
De plus, ce projet permettrait d’en apprendre davantage sur la pathologie, notamment grâce à l’identification de nouveaux biomarqueurs, lesquels ouvriraient la porte d’un autre progrès : diagnostiquer plus tôt la maladie de Charcot, notamment dans les familles comptant déjà un ou plusieurs membres concernés. L’occasion d’intervenir avant l’apparition des premiers symptômes, afin d’éviter que le processus neurodégénératif ne se mette en place et ne cause des dommages irréversibles. L’identification de biomarqueurs serait également précieuse pour prédire l’évolution de la maladie et prescrire le traitement le plus adapté en conséquence. Plusieurs essais cliniques sont en cours pour suivre cette piste.
La recherche se poursuit également dans le développement de nouveaux traitements. Un médicament qui a fait ses preuves aux Etats-Unis sur une certaine catégorie de patients est accessible en France, mais sous des conditions bien précises. D’autres études sont en cours et l’efficacité de nouveaux traitements potentiels reste à évaluer, qu’il s’agisse de médicaments ou de thérapie cellulaire (restaurer la fonction d’un tissu ou d’un organe malade en introduisant des cellules saines).
 Sauvegarder
Sauvegarder